El Ácido Sulfúrico: Un Compuesto Químico Industrial Esencial
Propiedades Físicas y Químicas
El ácido sulfúrico (H2SO4) es un líquido aceitoso y viscoso que exhibe una transparencia o un leve color amarillento característico. Su olor acre y penetrante se asemeja a "huevos podridos". Es altamente soluble en agua y posee una naturaleza deshidratante, extrayendo humedad del entorno. Como agente oxidante potente, reacciona con facilidad con los metales a altas temperaturas.
Aplicaciones Industriales
El ácido sulfúrico encuentra una amplia gama de usos en diversos sectores industriales. En la industria petroquímica, desempeña un papel crucial en el refinamiento del petróleo crudo. La agroquímica lo emplea extensamente para la producción de fertilizantes esenciales, como el fosfórico y el sulfato de amonio. Además, la industria química lo utiliza como precursor para la síntesis de otros productos químicos.
En la industria del papel y los textiles, el ácido sulfúrico se emplea en la fabricación de papel y el tratamiento de telas. Su capacidad para eliminar el óxido y proporcionar recubrimientos lo convierte en un componente valioso en la industria del tratamiento de metales. Finalmente, en la industria farmacéutica, es indispensable para la fabricación de medicamentos.
Beneficios para la Industria
Las innumerables aplicaciones del ácido sulfúrico brindan una amplia gama de beneficios a las industrias que lo utilizan. Su papel en la fabricación de otros productos químicos es fundamental para la cadena de suministro. En la refinación del petróleo, actúa como catalizador, acelerando los procesos y mejorando la eficiencia. Como base para los fertilizantes, promueve el crecimiento saludable de las plantas y aumenta los rendimientos agrícolas.
El ácido sulfúrico también mejora la limpieza y el mantenimiento, ya que se utiliza en limpiadores de desagües y otros productos de limpieza. Su naturaleza corrosiva lo hace eficaz para eliminar la suciedad y los residuos, lo que se traduce en un funcionamiento óptimo del equipo.
Peligros y Precauciones
El ácido sulfúrico es un compuesto altamente corrosivo y peligroso que requiere un manejo y almacenamiento cuidadosos. El contacto con la piel puede provocar quemaduras químicas graves, mientras que la inhalación puede dañar el sistema respiratorio. La reacción violenta con el agua genera calor intenso y salpicaduras, lo que plantea riesgos de lesiones.
Es esencial manipular el ácido sulfúrico con guantes, gafas y ropa protectora. Se debe almacenar en recipientes resistentes a la corrosión y alejado de materiales combustibles. Los derrames deben neutralizarse con jabón o agua de cal antes de lavarse con agua. La eliminación adecuada de la ropa y las joyas contaminadas es crucial para prevenir lesiones.
Manipulación y Almacenamiento Seguros
Para garantizar la seguridad, es fundamental seguir estrictamente los siguientes procedimientos:
- Nunca añadir agua al ácido sulfúrico (siempre añadir ácido al agua).
- Manipular con equipo de protección completo.
- Almacenar en recipientes diseñados para resistir la corrosión.
- Neutralizar los derrames antes de limpiarlos con agua.
- Eliminar la ropa y las joyas contaminadas.
- Implementar controles de calidad rigurosos para un uso seguro.
20 Puntos Relevantes sobre el Ácido Sulfúrico
- El ácido sulfúrico es el compuesto químico más producido a nivel mundial.
- Se utiliza principalmente en la producción de fertilizantes, otros ácidos y sulfatos.
- Se obtiene de la oxidación del dióxido de azufre (SO2) con óxidos de nitrógeno.
- Es un líquido corrosivo con una estructura molecular piramidal.
- Reacciona violentamente con el agua y los compuestos orgánicos, liberando calor.
- El descubrimiento del ácido sulfúrico se atribuye a Jabir ibn Hayyan en el siglo VIII.
- En la Edad Media, se conocía como aceite de vitriolo o vitriolo.
- John Roebuck industrializó su producción en cámaras de plomo en el siglo XVIII.
- El proceso de contacto, desarrollado en el siglo XIX, produce ácido sulfúrico más concentrado.
- El proceso de cámaras de plomo utiliza óxidos de nitrógeno como catalizadores.
- El proceso de contacto emplea platino u óxido de vanadio como catalizadores.
- El proceso de contacto tiene una mayor eficiencia de conversión (96-97%).
- Las impurezas en las piritas pueden envenenar el catalizador en el proceso de contacto.
- El ácido sulfúrico se utiliza en la producción de baterías, como las de los automóviles.
- Es crucial añadir ácido concentrado al agua (no al revés) para evitar salpicaduras peligrosas.
- El ácido sulfúrico es un ácido fuerte que se disocia en agua.
- Es un compuesto incoloro, pero a menudo se torna amarillo o marrón debido a las impurezas.
- Tiene una alta densidad (1,84 g/cm³) y un punto de ebullición de 337 °C.
- Es higroscópico, es decir, absorbe humedad del aire.
- El manejo del ácido sulfúrico requiere precauciones estrictas debido a su naturaleza corrosiva.
Anhídrido Sulfúrico (SO3) y Ácido Sulfúrico
El anhídrido sulfúrico (SO3) y el ácido sulfúrico son sustancias tóxicas que plantean riesgos para la salud humana.
Fuentes y Exposición:
Se encuentran en la industria química, la refinación de petróleo y la producción de baterías. La exposición puede ocurrir por inhalación, contacto con la piel o los ojos, o ingestión.
Efectos sobre la Salud:
El ácido sulfúrico causa quemaduras graves en la piel, los ojos, los pulmones y el tracto digestivo. La exposición a altas concentraciones puede ser fatal. La exposición crónica puede provocar cáncer de laringe.
Efectos en los Niños:
Los niños son más susceptibles a los efectos del ácido sulfúrico debido a sus vías respiratorias más pequeñas y mayor tasa de respiración.
Prevención y Control:
- Mantener los productos químicos fuera del alcance de los niños.
- Usar equipo de protección al manipular sustancias que contienen SO3 y ácido sulfúrico.
- Limitar las emisiones de SO3 para reducir la formación de ácido sulfúrico en el aire.
- Establecer límites de exposición ocupacional para el ácido sulfúrico en el lugar de trabajo.
| Categoría | Características, Consejos o Puntos Clave |
|---|---|
| Propiedades Físicas y Químicas | |
| Líquido: Aceitoso y viscoso | |
| Color: Transparente o ligeramente amarillo | |
| Olor: A "huevos podridos" | |
| Soluble: En agua | |
| Efecto deshidratante: Absorbe humedad | |
| Agente oxidante: Reacciona con metales | |
| Aplicaciones Industriales | |
| Industria petroquímica: Refinación de petróleo crudo | |
| Agroquímica: Producción de fertilizantes | |
| Industria química: Síntesis de otros productos químicos | |
| Industria del papel y los textiles: Fabricación de papel y tratamiento de textiles | |
| Tratamiento de metales: Eliminación de óxido y recubrimiento | |
| Industria farmacéutica: Fabricación de medicamentos | |
| Beneficios para la Industria | |
| Fabricación: De otros productos químicos | |
| Catálisis: En refinación de petróleo | |
| Producción de fertilizantes: Mejora el crecimiento de las plantas | |
| Limpieza y mantenimiento: Limpiadores de desagües | |
| Peligros y Precauciones | |
| Contacto con la piel: Quemaduras químicas graves | |
| Contacto con los ojos: Daño permanente y ceguera | |
| Inhalación: Dificultad para respirar y ardor en el sistema respiratorio | |
| Riesgo de incendio: Combustible en combinación con otros materiales | |
| Manipulación y Almacenamiento Seguros | |
| Nunca añadir agua al ácido: Siempre añadir ácido al agua | |
| Manipular con equipo de protección: Guantes, gafas y ropa protectora | |
| Almacenar en recipientes resistentes a la corrosión: | |
| Neutralizar derrames con jabón o agua de cal: Antes de lavar con agua | |
| Eliminar ropa y joyas contaminadas: | |
| Seguimiento de estrictos controles de calidad: Para garantizar el uso seguro | 20 Puntos Relevantes sobre el Ácido Sulfúrico |
| 1: Compuesto químico más producido en el mundo | |
| 2: Usado en fertilizantes, ácidos y sulfatos | |
| 3: Obtenido de dióxido de azufre mediante oxidación | |
| 4: Líquido corrosivo con estructura piramidal | |
| 5: Reacciona violentamente con agua y materia orgánica | |
| 6: Descubierto por Jabir ibn Hayyan en el siglo VIII | |
| 7: Conocido como aceite o vitriolo en la Edad Media | |
| 8: Industrializado por John Roebuck en el siglo XVIII | |
| 9: El proceso de contacto produce ácido más concentrado | |
| 10: El proceso de cámaras de plomo usa óxidos de nitrógeno como catalizadores | |
| 11: El proceso de contacto emplea platino u óxido de vanadio | |
| 12: El proceso de contacto tiene mayor eficiencia de conversión | |
| 13: Las impurezas pueden envenenar el catalizador en el proceso de contacto | |
| 14: Usado en baterías, como las de automóviles | |
| 15: Añadir ácido al agua (no al revés) evita salpicaduras | |
| 16: Ácido fuerte que se disocia en agua | |
| 17: Incoloro, pero puede tornarse amarillo o marrón por impurezas | |
| 18: Alta densidad y punto de ebullición | |
| 19: Higroscópico (absorbe humedad) | |
| 20: Requiere precauciones estrictas para su manipulación | Anhídrido Sulfúrico (SO3) y Ácido Sulfúrico |
| Fuentes: Industria química, refinación de petróleo, producción de baterías | |
| Exposición: Respiración, contacto con la piel/ojos, ingestión | |
| Efectos sobre la Salud: Quemaduras graves, exposición fatal a altas concentraciones, cáncer de laringe | |
| Efectos en Niños: Susceptibles debido a vías respiratorias más pequeñas y mayor tasa de respiración | |
| Prevención y Control: Mantener productos químicos fuera del alcance de los niños, usar equipo de protección, límites de exposición ocupacional | |
| Medidas del Gobierno: Límites de emisiones de SO3, límites de exposición en el lugar de trabajo |
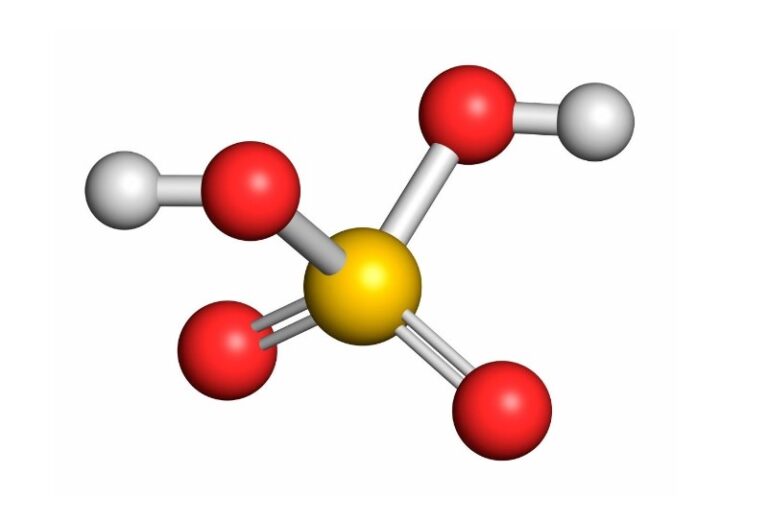
¿Qué es el ácido sulfúrico?
Es un compuesto químico altamente versátil y ampliamente utilizado en diversas industrias.
¿Cuáles son sus propiedades físicas?
- Líquido aceitoso y viscoso
- Transparente o ligeramente amarillo
- Olor a "huevos podridos"
- Soluble en agua
- Efecto deshidratante
¿Cuáles son sus propiedades químicas?
- Agente oxidante potente
- Reacciona con metales a altas temperaturas
¿En qué industrias se utiliza?
- Industria petroquímica
- Agroquímica
- Industria química
- Industria del papel y los textiles
- Tratamiento de metales
- Industria farmacéutica
¿Cuáles son sus beneficios para la industria?
- Fabricación de otros productos químicos
- Catálisis en refinación de petróleo
- Producción de fertilizantes
- Mejora del crecimiento de las plantas
- Limpieza y mantenimiento
¿Cuáles son sus peligros?
- Contacto con la piel: Quemaduras químicas graves
- Contacto con los ojos: Daño permanente y ceguera
- Inhalación: Dificultad para respirar y ardor en el sistema respiratorio
- Riesgo de incendio: Combustible en combinación con otros materiales
¿Cómo se manipula y almacena de forma segura?
- Nunca añadir agua al ácido sulfúrico (siempre añadir ácido al agua)
- Manipular con guantes, gafas y ropa protectora
- Almacenar en recipientes resistentes a la corrosión
- Neutralizar derrames con jabón o agua de cal antes de lavar con agua
- Eliminar ropa y joyas contaminadas
- Seguir estrictos controles de calidad para garantizar el uso seguro
